Silic - Chuyên đề Hóa 11
I. Silic
1. Tính chất vật lý
- Silic có 2 dạng thù hình: Silic tinh thể và silic vô định hình.
2. Tính chất hóa học
- Silic có các số oxi hóa: -4,0, +2 và +4 (số oxi hóa +2 ít đặc trưng hơn).
- Trong các phản ứng hóa học, silic vừa thể hiện tính oxi hóa vừa thể hiện tính khử.
a. Tính khử:
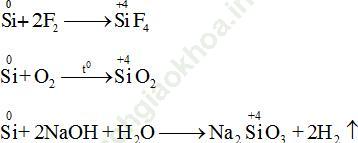
b. Tính oxi hóa
Mg + Si to→ Mg2Si
3. Điều chế
- Khử SiO2 ở nhiệt độ cao
SiO2 + 2Mg to → Si + MgO
II. HỢP CHẤT CỦA SILIC
1. Silic đioxit
- SiO2 là chất ở dạng tinh thể.
- Tan chậm trong dung dịch kiềm đặc nóng, tan dễ trong kiềm nóng chảy.
SiO2 + 2NaOH → Na2SiO3 + H2O
- Tan được trong axit HF
SiO2 + 4HF → SiF4 + 2H2O
- Dựa vào tính chất này, người ta dùng dung dịch HF để khắc chữ lên thủy tinh.
2. Axit silixic
- H2SiO3 là chất ở dạng keo, không tan trong nước. Khi mất một phần nước tạo thành vật liệu xốp là silicagen. Dùng để hút hơi ẩm trong các thùng đựng hàng hóa.
- Axit silixic là axit yếu, yếu hơn cả axit cacbinic nên bị axit này đẩy ra khỏi dung dịch muối.
Na2SiO3 + CO2 + H2O → Na2CO3 + H2SiO3↓
3. Muối silicat
- Đa số các muối silicat đều không tan, chỉ có muối silicat của kim loại kiềm tan được trong nước.
- Dung dịch đậm đặc của Na2SiO3 và K2SiO3 được gọi là thủy tinh lỏng.
Bài trước: Axit cacbonic và muối cacbonat - Chuyên đề Hóa 11 Bài tiếp: Tính khử của CO - Chuyên đề Hóa 11