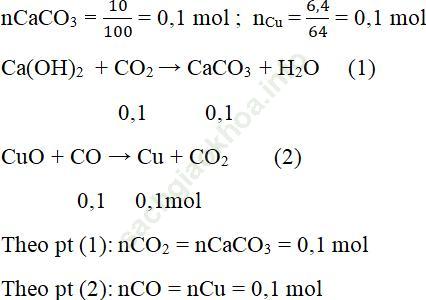Bài 21: Hợp chất của cacbon - Giải BT Hóa học 11 nâng cao
Bài 21: Hợp chất của cacbon
Bài 1 (trang 87 sgk Hóa 11 nâng cao): Khi nung nóng kẽm oxit với than cốc thì tạo thành một chất khí cháy được. viết Phương trình hóa học.
Bài giải:Bài 2 (trang 88 sgk Hóa 11 nâng cao): Làm thế nào để tách riêng từng khí CO và CO2 ra khỏi hỗn hợp của chúng:
a) Bằng Phương pháp vật lí
b) Bằng Phương pháp hóa học
Bài giải:a) Tách riêng từng khí CO và CO2 ra khỏi hỗn hợp của chúng bằng phương pháp vật lí như sau:
- Nén dưới áp suất cao, CO2 hóa lỏng, tách riêng được CO2 và CO ra khỏi nhau.
b) Tách riêng từng khí CO và CO2 ra khỏi hỗn hợp của chúng bằng phương pháp hóa học như sau:
- Dẫn hỗn hợp đi qua dung dịch Ca (OH)2 dư, CO2 bị hấp thụ, thu được CO thoát ra.
Phương trình: CO2+Ca (OH)2→ CaCO3 +H2O
- Lọc kết tủa, hòa tan kết tủa trong dung dịch HCl, dẫn khí tạo thành qua NaHCO3 loại bỏi HCl thu CO2
Phương trình: CaCO3+2HCl→ CaCl2+CO2+H2O
Bài 3 (trang 88 sgk Hóa 11 nâng cao):
a) Làm thế nào để loại các tạp chất là hơi nước và CO2 có trong CO?
b) làm thế nào để chuyển NaHCO3 thành Na2CO3, Ca (HCO3)2 thành CaCO3 và ngược lại?
Bài giải:a) Để loại tạp chất là hơi nước và CO2 có trong khí CO ta dẫn hỗn hợp trên vào dung dịch Ca (OH)2 dư, CO2 và H2O bị hấp thụ, ta thu được CO.
CO2 + Ca (OH)2 → CaCO3 + H2O
b)
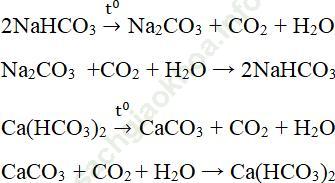
Bài 4 (trang 88 sgk Hóa 11 nâng cao): Có một hỗn hợp khí gồm cacbon đioxit và lưu huỳnh đioxit. Bằng phương pháp hóa học hãy chứng minh sự có mặt của mỗi khí trong hỗn hợp.
Bài giải:Chứng minh sự có mặt CO2, SO2 trong hỗn hợp:
- Dẫn hỗn hợp trên qua dung dịch Br2 dư
Nếu dung dịch Br2 bị mất màu ⇒ hỗn hợp có chứa SO2.
PTHH: SO2+Br2+2H2O→ H2SO4+2HBr
- Dẫn khí còn lại qua dung dịch Ca (OH)2 dư
Nếu thấy có kết tủa trắng ⇒ hỗn hợp có CO2.
PTHH: CO2+Ca (OH)2→ CaCO3+H2O
Bài 5 (trang 88 sgk Hóa 11 nâng cao): Dung dịch nước của chất A làm quỳ tím hóa xanh, còn dung dịch nước của chất B không đổi màu quỳ tím. Trộn lẫn dung dịch của hai chất lại thì xuất hiện kết tủa. A và B có thể là:
A. NaOH và K2SO4
B. K2CO3 và Ba (NO3)2
C. KOH và FeCl3
D. Na2CO3 và KNO3
Bài giải:Đáp án đúng là: B.
- Dung dịch K2CO3 làm quỳ tím hóa xanh vì tạo từ bazơ mạnh và axit yếu.
- Dung dịch Ba (NO3)2 không làm đổi màu quỳ tím vì tạo từ axit mạnh và bazơ mạnh.
- Trộn 2 dd trên ta thu được kết tủa là BaCO3
PTHH: K2CO3+Ba (NO3)2→ BaCO3↓ +2KNO3
Bài 6 (trang 88 sgk Hóa 11 nâng cao): Xác định thành phần phần trăm (về thể tích) của hỗn hợp khí gồm N2, CO và CO2, biết rằng khi cho 10 lít (đktc) hỗn hợp khí đó đi qua một lượng dư nước vôi trong, rồi qua đồng (II) oxit dư đốt nóng, thì thu được 10,0g kết tủa và 6,4g đồng. Nếu cũng lấy 10,0 lít (đktc) hỗn hợp khí đó cho đi qua ống đựng đồng (II) axit dư đốt nóng, rồi đi qua một lượng dư nước vôi trong thì thu được bao nhiêu gam kết tủa?
Bài giải: