Dạng 7: Bài tập về nhóm Halogen - Chuyên đề Hóa 10
A. Bài tập tự luận
Ví dụ 1: Điện phân nóng chảy một muối 11,7g halogenua NaX người ta thu được 2,24 lít khí (đktc).
a) Xác định nguyên tố X?
b) Tính thế tích khí HX thu được khi cho X tác dụng với 4,48 lít H2 ở đktc?
c) Tính tỷ lệ % các khí sau phản ứng?
Bài giải:
Phương trình phản ứng xảy ra:
2NaX → 2Na + X2
a, nX2 = 0,1 mol ⇒ nNaX = 2.0,1 = 0,2 mol.
MNaX = 11,7/0,2 = 58,5 ⇒ X = 35,5 (Cl)
b, X2 + H2 → 2HX
nH2 = 0,2 mol ⇒ nHX = 2. nX2= 0,2 mol (H2 dư)
⇒ VHX = 0,2.22,4 = 4,48 l
c, Sau phản ứng có 0,2 mol khí HCl và 0,1 mol H2 dư
%HCl= 0,2/ (0,2 + 0,1)= 66,67%
⇒ %H2 = 33,33%
Ví dụ 2. Nung 12,87 g NaCl với H2SO4 đặc, dư thu được bao nhiêu lít khí ở đktc và bao nhiêu gam muối Na2SO4. Biết rằng hiệu suất của phản ứng là H = 90%.
Bài giải:
Phương trình phản ứng xảy ra như sau:
2NaCl + H2SO4 → Na2SO4 + HCl
nNaCl = 12,87 / 58,5 =0,22 mol
⇒ nNa2SO4 = 0,11 mol
⇒ mNa2SO4 = 0,11.142.90% = 14,058 g.
Ví dụ 3. Cho 31,6 g KMnO4 tác dụng với dung dịch HCl dư sẽ thu được bao nhiêu lít Cl2 (ở đktc) nếu H của phản ứng là 75%.
Bài giải:
Phương trình phản ứng xảy ra như sau:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
nKMnO4 = 31,6/ 158 = 0,2 mol
nCl2 = 0,2.5/2= 0,5 mol
⇒ VCl2 = 0,5.22,4.75% = 8,4 l
Vậy số lít khí Cl2 thu được (ở đktc) là: 8,4 l
Ví dụ 4. Cho 0,896 lít Cl2 tác dụng với 200 ml dung dịch NaOH 1M ở to thường thu được dung dịch X. Tính CM của các chất trong dung dịch X?
Bài giải:
Phương trình phản ứng xảy ra như sau:
Cl2 + 2NaOH → NaCl + NaClO + H2O
nCl2 = 0,896/22,4 = 0,04 mol
nNaOH = 0,2 mol
Theo phương trình ta có: nNaCl = nNaClO = nCl2 =0,04 mol
⇒ CMNaCl = CMNaClO = 0,04/0,2 = 0,2M
nNaOHdư = 0,2 – 0,04.2 = 0,12 mol
⇒ CMNaOH = 0,12 / 0,2 = 0,6M
B. Bài tập trắc nghiệm
Câu 1. Cho 17,4 gam MnO2 tác dụng hết với HCl lấy dư. Toàn bộ khí clo sinh ra được hấp thụ hết vào 148,5 gam dung dịch NaOH 20% (ở nhiệt độ thường) tạo ra dung dịch A. Vậy dung dịch A có các chất và nồng độ % tương ứng là?
A. NaCl 10%; NaClO 5%
B. NaCl 7,31%; NaClO 6,81%, NaOH 6%
C. NaCl 7,19%; NaClO 9,16%, NaOH 8,42%
D. NaCl 7,31%; NaClO 9,31%, HCl 5%
Đáp án: A
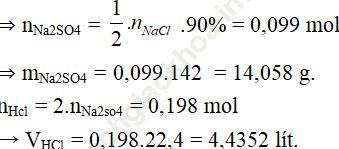
Câu 2. Hidro clorua bị oxi hóa bởi MnO2 biết rằng khí clo tạo thành trong phản ứng đó có thể đẩy được 12,7 gam iot từ dung dịch natri iotua. Tính khối lượng HCl là bao nhiêu?
A. 7,3g B. 14,6g C. 3,65g D. 8,9g
Đáp án: A
Phương trình phản ứng:
MnO2 + 4HCl → MnCl2 + Cl2 + H2O
0,2 0,05 mol
Cl2 + 2KI → 2KCl + I2
0,05 0,05
mHCl = 0,2 × 36,5 = 7,3g
Câu 3. Nguyên tố R là phi kim thuộc phân nhóm chính trong bảng tuần hoàn. Tỷ lệ % R trong oxit cao nhất với %R trong hợp chất khí với hidro là 0,5955. Tìm R?
A. Flo B. Clo C. Brom D. Iot
Đáp án: C
Gọi công thức của R với oxi là R2Ox (x = 4,5,6,7)
Suy ra công thức của R với hidro là RH8 – x
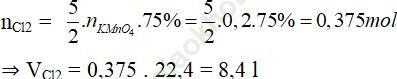
→ Rút ra được biểu thức liên hệ R và x
Sau đó biện luận ta được x = 7, R = 80 → R là Brom
Câu 4. Cho 19,05 gam hỗn hợp KF và KCl tác dụng hết với dung dịch H2SO4 đặc thu được 6,72 lít khí (đktc). Tính % theo khối lượng của KF và KCl?
A. 60,20% và 39,80%
B. 60,89% và 39,11%
C. 39,11% và 60,89%
D. 70% và 30%
Đáp án: B

Câu 5. Dung dịch A chứa đồng thời axit HCl và H2SO4. Để trung hòa 40 ml A cần dùng vừa hết 60 ml NaOH 1M. Cô cạn dung dịch khi trung hòa, thu được 3,76 g hỗn hợp muối khan. Tính nồng độ mol/l của 2 axit HCl và H2SO4?
A. 1 và 0,75 B. 0,25 và 1 C. 0,25 và 0,75 D. 1 và 0,25
Đáp án: D
Gọi a, b là nồng độ mol của HCl và H2SO4
HCl + NaOH → NaCl + H2O
0,04a 0,04a 0,04a
H2SO4 + 2NaOH → Na2SO4 + 2H2O
0,04b 0,08b 0,04b

Câu 6. Khi đun nóng muối kali clorat, không có xúc tác, thì muối này bị phân hủy đồng thời theo hai phương trình sau đây:
2KClO3 → 2KCl + 3O2 (1)
4KClO3 → 3KClO3 + KCl (2)
Biết rằng khi phân hủy hoàn toàn 73,5 gam kali clorat thì thu được 33,5 gam kali clorua. Tính phần trăm khối lượng KClO3 phân hủy theo (1)?
A. 80,23% B. 83,25% C. 85,1% D. 66,67%
Đáp án: D
Các phản ứng xảy ra: