Dạng 3: Cách viết công thức cấu tạo của các phân tử - Chuyên đề Hóa 10
A. Phương pháp & Ví dụ
Lý thuyết và Phương pháp giải
- Viết cấu hình electron của các nguyên tử tạo hợp chất
- Tính nhẩm số electron mỗi nguyên tử góp chung = 8 – số electron lớp ngoài cùng
- Biểu diễn các electron lớp ngoài cùng và các cặp electron chung (bằng các dấu chấm) lên xung quanh kí hiệu nguyên tử ⇒ Công thức của electron.
- Thay mỗi cặp electron chung bằng 1 gạch ngang ta được công thức cấu tạo.
Chú ý:
- Khi 2 nguyên tử liên kết mà trong đó có một nguyên tử A đạt cấu hình bền còn nguyên tử B kia chưa thì lúc này A sử dụng cặp electron của nó để cho B dùng chung → hình thành liên kết cho nhận (hay phối trí) biểu diễn bằng → hướng vào nguyên tử nhận cặp electron đó.
- Khi có nhiều nguyên tử đều có thể đưa cặp electron ra cho nguyên tử khác dùng chung thì ưu tiên cho nguyên tử nào có độ âm điện nhỏ hơn.
- Khi viết công thức cấu tạo công thức cấu tạo của:
* Axit có oxi: theo thứ tự
+ Viết có nhóm H – O
+ Cho O của nhóm H – O liên kết với phi kim trung tâm
+ Sau đó cho phi kim trung tâm liên kết với O còn lại nếu có.
* Muối:
+ Viết công thức cấu tạo của axit tương ứng trước.
+ Sau đó thay H ở axit bằng kim loại.
Ví dụ minh họa
Ví dụ 1. Trình bày sự hình thành liên kết cho nhận trong các phân tử và sau H3O+, HNO3
Bài giải:
- Xét phân tử H3O+ ta có:

- Xét phân tử HNO3 ta có:
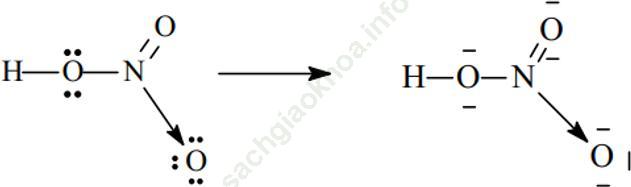
Sau khi hình thành các liên kết cộng hóa trị, N (chứ không phải O) sẽ cho 1 cặp e đến nguyên tử O thứ ba (đang thiếu 2e để đạt cấu hình khí trơ) hình thành liên kết cho - nhận.
Lưu ý:
- Cấu tạo phân tử và biểu diễn với liên kết cho nhận là để phù hợp với quy tắc bát tử.
- Với nguyên tử cho cặp e có 3 lớp trở lên, có thể có hóa trị lớn hơn 4 nên còn biểu diễn bằng liên kết cộng hóa trị.
Ví dụ 2: Viết công thức cấu tạo (CTCT) của phân tử H2SO4 và HClO4 để thấy được quy tắc bát tử chỉ đúng với 1 số trường hợp.
Bài giải:
Công thức cấu tạo của phân tử H2SO4 và HClO4 như sau:
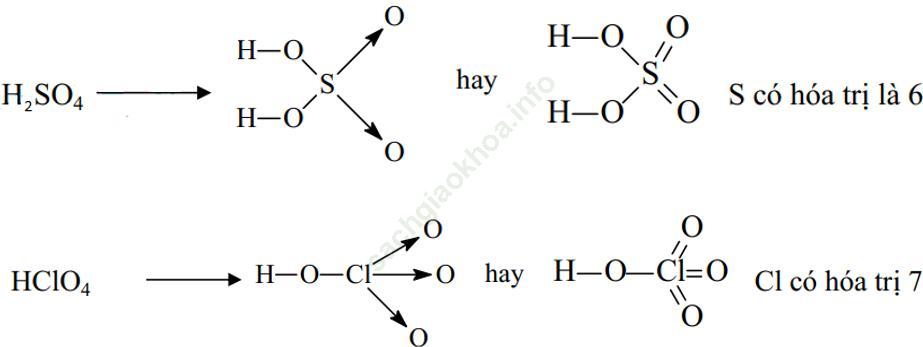
Ví dụ 3: Viết công thức electron và CTCT các ion đa nguyên tử sau: CO32-, HCO3-
Bài giải:
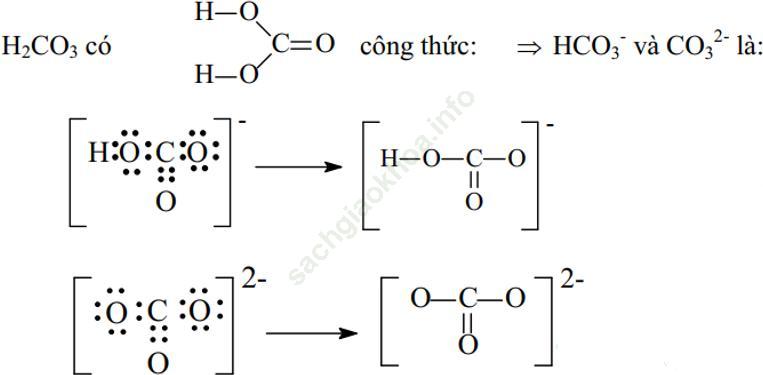
Ví dụ 4. Viết công thức cấu tạo của các chất sau: Cl2O, Cl2O5,HClO3.
Bài giải:
Công thức cấu tạo của các chất Cl2O, Cl2O5,HClO3 như sau:
+) Cl2O:
+) Cl2O5:

+) HClO3:
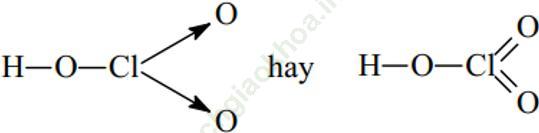
B. Bài tập trắc nghiệm
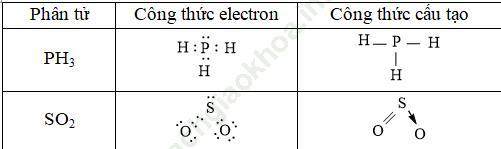
Câu 1. Hãy viết công thức e và CTCT của các phân tử sau: PH3, SO2
Công thức e và CTCT của các phân tử sau: PH3, SO2
Câu 2. Viết công thức electron, CTCT của: HClO, HCN, HNO2.
Công thức electron, CTCT của: HClO, HCN, HNO2.

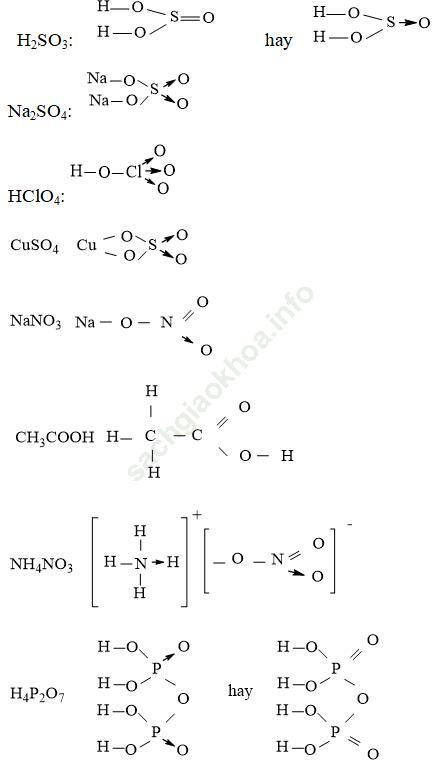
Câu 3. Viết CTCT của các phân tử và ion sau: H2SO3, Na2SO4, HClO4, CuSO4, NaNO3, CH3COOH, NH4NO3, H4P2O7.
CTCT của các phân tử và ion của H2SO3, Na2SO4, HClO4, CuSO4, NaNO3, CH3COOH, NH4NO3, H4P2O7.
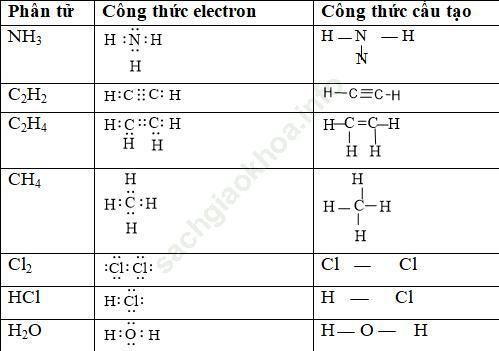
Câu 4. Viết công thức electron, CTCT của các phân tử: NH3, C2H2, C2H4, CH4, Cl2, HCl, H2O.
Công thức electron, CTCT của các phân tử: NH3, C2H2, C2H4, CH4, Cl2, HCl, H2O.
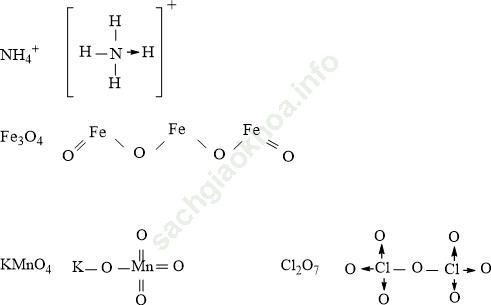
Câu 5. Viết CTCT của các phân tử và ion sau: NH4+, Fe3O4, KMnO4, Cl2O7
CTCT của các phân tử và ion sau: NH4+, Fe3O4, KMnO4, Cl2O7
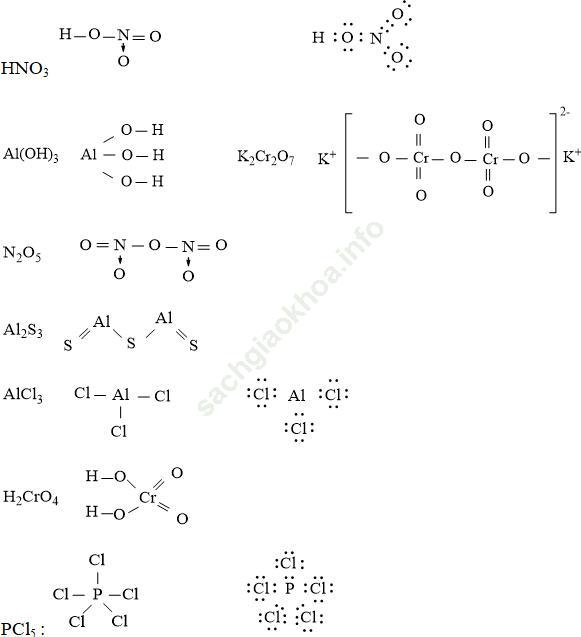
Câu 6. Viết công thức electron và CTCT các chất sau: HNO3, Al (OH)3, K2Cr2O7, N2O5, Al2S3, H2CrO4, PCl5
Công thức electron và CTCT của HNO3, Al (OH)3, K2Cr2O7, N2O5, Al2S3, H2CrO4, PCl5