4 dạng bài tập Nguyên tử Hóa 10 trong đề thi Đại học có lời giải - Chuyên đề Hóa 10
4 dạng bài tập Nguyên tử Hóa 10 trong đề thi Đại học có lời giải
Dạng 1: Bài tập về thành phần của nguyên tử
Phương pháp giải
+ Nguyên tử gồm: Hạt nhân (hạt proton và nơtron) và vỏ nguyên tử (các hạt electron)
+ Nguyên tử được cấu tạo từ 3 loại hạt cơ bản đó là: hạt electron, proton và nơtron.
+ Số đơn vị điện tích hạt nhân = số proton = số electron (Z = P = E)
+ Số khối A của hạt nhân: là tổng số proton Z và số nơtron N (A = Z + N)
+ Khối lượng nguyên tử bằng tổng khối lượng proton, notron và electron. Vì khối lượng electron rất nhỏ nên có thể coi khối lượng nguyên tử bằng khối lượng hạt nhân.
+ Nguyên tố hóa học là những nguyên tử có cùng điện tích hạt nhân.
Ví dụ minh họa
Ví dụ 1: Phát biểu nào sau đây là không đúng?
A. Nguyên tử được cấu tạo từ các hạt cơ bản là p, n, e.
B. Nguyên tử có cấu trúc đặc khít, gồm vỏ nguyên tử và hạt nhân nguyên tử.
C. Hạt nhân nguyên tử cấu tạo bởi các hạt proton và hạt nơtron.
D. Vỏ nguyên tử được cấu tạo từ các hạt electron.
Bài giải:
Phát biểu không đúng là: D
Ví dụ 2: Nguyên tố hóa học bao gồm các nguyên tử:
A. Có cùng số khối A
B. Có cùng số proton
C. Có cùng số nơtron
D. Có cùng số proton và số nơtron
Bài giải:
Đáp án đúng là: B
Ví dụ 3: Hạt nhân của hầu hết các nguyên tử do các loại hạt... cấu tạo nên.
A. electron, proton và nơtron
B. electron và nơtron
C. proton và nơtron
D. electron và proton
Bài giải:
Đáp án đúng là: A
Ví dụ 4: Cặp phát biểu nào sau đây là đúng:
1. Obitan nguyên tử là vùng không gian quanh hạt nhân, ở đó xác suất hiện diện của electron là rất lớn (trên 90%).
2. Đám mây electron không có ranh giới rõ rệt còn obitan nguyên tử có ranh giới rõ rệt.
3. Mỗi obitan nguyên tử chứa tối đa 2 electron với chiều tự quay giống nhau.
4. Trong cùng một phân lớp, các electron sẽ được phân bố trên các obitan sao cho các electron độc thân là tối đa và các electron phải có chiều tự quay khác nhau.
5. Mỗi obitan nguyên tử chứa tối đa 2 electron với chiều tự quay khác nhau.
A. 2,4,5.
B. 2,3.
C. 3,4.
D. 2,3,4.
Bài giải:
Đáp án đúng là: D
Ví dụ 5: Chọn câu phát biểu sai:
1. Trong một nguyên tử luôn luôn có số prôtôn = số electron = số điện tích hạt nhân
2. Tổng số prôton và số electron trong một hạt nhân gọi là số khối
3. Số khối A là khối lượng tuyệt đối của nguyên tử
4. Số prôton = điện tích hạt nhân
5. Đồng vị là các nguyên tử có cùng số prôton nhưng khác nhau về số nơtron
A. 1,3,5.
B. 3,2,4.
C. 3,5,4.
D. 1,2,5.
Bài giải:
Câu phát biểu sai là: 2,3,4
⇒ Đáp án cần chọn là: B
Dạng 2: Tìm số P, E, N, số khối A – Viết kí hiệu nguyên tử
Phương pháp giải
Kí hiệu nguyên tử: ![]()
Để tìm được số các hạt và tính số khối ta thường sử dụng các công thức sau:
Z = P = E
A = Z + N
P ≤ N ≤ 1,5P
Ví dụ minh họa
Ví dụ 1: Nguyên tử Nhôm có điện tích hạt nhân là 13+. Trong nguyên tử nhôm số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt. Tính số khối của nhôm?
A. 13
B. 14
C. 27
D. 26
Bài giải:
Điện tích hạt nhân của Al là: 13+ ⇒ p = 13
Số hạt mang điện là p và e; số hạt không mang điện là n
⇒ p + e – n = 12
Mà p = e ⇒ 2p – e = 12
Thay p = 13 ⇒ n = 26 – 12 = 14
⇒ A = p + n = 13 + 14 = 27
⇒ Đáp án đúng là: C
Ví dụ 2: Biết nguyên tử B có tổng số hạt là 21. Số hạt không mang điện chiếm 33,33%. Kí hiệu nguyên tử của B là?
Bài giải:
Số hạt không mang điện chiếm 33,33% ⇒ % n = 33,33;
Tổng số hạt = 21
⇒ n = 33,33%. 21 = 7 (1)
Ta có: p + n + e = 21
Mà p = e ⇒ 2p + n = 21 (2)
Thay n = 21 ⇒ p = e = (21−7): 2 = 7
A = p + n = 7 + 7 = 14; Z = p = e = 7
⇒ Kí hiệu nguyên tử B là: ![]()
⇒ Đáp án đúng là: A
Ví dụ 3: Tổng số hạt trong nguyên tử X là 28. Cho biêt số hạt p, n, e của X là?
A. 8; 12; 8
B. 9; 10; 9
C. Không xác định được
D. Cả A và B
Bài giải:
Tổng số hạt = 28
⇒ p + n + e = 28
⇒ 2p + n = 28
Ta có: p < n < 1,5p
⇒ 3p ≤ 2p + n = 28 ≤ 3,5p
⇒ 8 ≤ p ≤ 9,3 mà p ∈ N
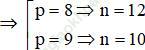
⇒ Đáp án đúng là: D
Ví dụ 4: Oxit X có công thức phân tử là R2O. Tổng số hạt cơ bản (p, n, e) trong X là 92. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 28. X là chất nào dưới đây. Biết rằng trong hạt nhân nguyên tử oxi có 8 proton và 8 nơtron.
A. N2O.
B. Na2O.
C. Cl2O.
D. K2O.
Bài giải:
Tổng số hạt cơ bản (p, n, e) trong X là 92
⇒ 2. (2pR + nR) + 2pO + nO = 92
Ta có: pO = 8; nO = 8
⇒ 2. (2pR + nR) = 68 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 28
⇒ (2.2pR + 2. nO) - (2nR + nO) = 28
⇒ 4pR - 2nR = 20 (2)
Từ (1) và (2) ⇒ pR = 11, nR = 12
⇒ R là Na
⇒ Đáp án đúng là: B
Dạng 3: Xác định nguyên tử khối trung bình, số khối, % các đồng vị
Phương pháp giải
+ Các đồng vị của cùng một nguyên tố là những nguyên tử có cùng số p nhưng khác nhau về số n. Vì vậy số khối A khác nhau.
+ Hầu hết các nguyên tố hóa học là hỗn hợp của nhiều đồng vị với tỉ lệ phần trăm số nguyên tử xác định ⇒ Nguyên tử khối của các nguyên tố có nhiều đồng vị là nguyên tử khối trung bình của hỗn hợp các đồng vị có tính đến tỉ lệ phần trăm số nguyên tử tương ứng.
Trong đó: ![]() là nguyên tử khối trung bình
là nguyên tử khối trung bình
A: là nguyên tử khối của đồng vị A, a là tỉ lệ phần trăm số nguyên tử của đồng vị A.
B: là nguyên tử khối của đồng vị B, b là tỉ lệ phần trăm số nguyên tử của đồng vị B.
Ví dụ minh họa
Ví dụ 1: Gali (với khối lượng nguyên tử là 69,72) trong tự nhiên là hỗn hợp hai đồng vị. Trong đó, đồng vị 69Ga có khối lượng nguyên tử là 68,9257 chiếm 60,47%. Khối lượng nguyên tử của đồng vị còn lại là bao nhiêu?
A. 69,9913.
B. 70,2163.
C. 70,9351.
D. 71,2158.
Bài giải:
Gọi khối lượng nguyên tử của đồng vị còn lại là M
Ta có: ![]()
⇒ M = 70,9351
⇒ Đáp án đúng là: C
Ví dụ 2: Nguyên tố X có 3 đồng vị: A1 chiếm 92,3%, A2 chiếm 4,7% và A3 chiếm 3%. Tổng số khối của 3 đồng vị là 87. Số n trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt. Nguyên tử khối trung bình của X là 28,107. Vậy số khối của 3 đồng vị là bao nhiêu?
A. 27,28,32.
B. 26,27,34.
C. 28,29,30.
D. 29,30,28.
Bài giải:
Gọi số khối của X lần lượt là A1, A2, A3
A1; A2; A3 là đồng vị nên có số p bằng nhau
Số n trong 1 nguyên tử A2 nhiều hơn trong nguyên tử A1 là một hạt
⇒ A2 – A1 = 1
Ta có hệ phương trình như sau:
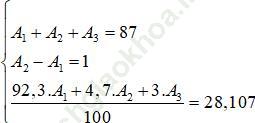
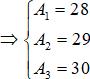
⇒ Đáp án đúng là: C
Ví dụ 3: Cho 5,85 gam muối NaX tác dụng với dung dịch AgNO3 dư ta thu được 14,35 gam kết tủa trắng. Nguyên tố X có hai đồng vị 35X (x1%) và 37X (x2%). Tìm giá trị của x1% và x2%?
A. 25% & 75%.
B. 75% & 25%.
C. 65% & 35%.
D. 35% & 65%.
Bài giải:
Khi cho NaX vào AgNO3 thu được kết tủa là AgX
Có: nNaX = nAgX
Ta có hệ:
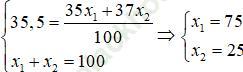
⇒ Đáp án đúng là: B
Ví dụ 4: Nguyên tố Cl có hai đồng vị bền với tỉ lệ phần trăm số nguyên tử tương ứng là:![]() chiếm 75,77% và
chiếm 75,77% và ![]() chiếm 24,23%. Trong phân tử CaCl2, % khối lượng của
chiếm 24,23%. Trong phân tử CaCl2, % khối lượng của ![]() là (biết nguyên tử khối trung bình của canxi là 40)?
là (biết nguyên tử khối trung bình của canxi là 40)?
A. ≈ 23,89.
B. ≈ 47,79.
C. ≈ 16,15.
D. ≈ 75,77.
Bài giải:
⇒ Đáp án đúng là: B
Dạng 4: Tìm nguyên tố viết cấu hình electron của nguyên tử
Phương pháp giải
+ Z là đại lượng đặc trưng cho nguyên tố hóa học nên để xác định nguyên tố ta cần xác định giá trị của Z.
+ Viết cấu hình electron: Các electron được phân bố theo thứ tự tăng dần mức năng lượng AO, theo các nguyên lí và quy tắc phân bố electron trong nguyên tử.
Ví dụ minh họa
Ví dụ 1: Một nguyên tử R có tổng số hạt mang điện và không mang điện là 34. Trong đó số hạt mang điện gấp 1,833 lần số hạt không mang điện. Nguyên tố R và cấu hình electron là bao nhiêu?
A. Na, 1s22s22p63s1.
B. Mg, 1s22s22p63s1.
C. Na, 1s22s22p63s2.
D. Mg, 1s22s22p63s2.
Bài giải:
Một nguyên tử R có tổng số hạt mang điện và không mang điện là 34.
⇒ 2p + n = 34 (1)
Số hạt mang điện gấp 1,833 lần số hạt không mang điện
⇒ 2p = 1,883n (2)
Từ (1) và (2) ⇒ p = 11, n = 12
⇒ R là nguyên tố Na
Cấu hình của Na như sau: 1s22s22p63s1.
⇒ Đáp án đúng là: A
Ví dụ 2: Tổng số các hạt p, n và hạt e trong nguyên tử của một nguyên tố là 40. Biết số hạt n> p là 1. Cho biết nguyên tố trên thuộc loại nguyên tố nào?
A. Nguyên tố s.
B. Nguyên tố p.
C. Nguyên tố d.
D. Nguyên tố f.
Bài giải:
Giả sử số hiệu nguyên tử, số n của nguyên tố trên lần lượt là Z, N
Ta có hệ phương trình như sau:
Cấu hình e của nguyên tố là: 1s22s22p63s23p1
Nhận thấy e cuối cùng điền vào phân lớp p
⇒ Nguyên tố trên thuộc loại nguyên tố p
⇒ Đáp án đúng là: B
Ví dụ 3: Cho nguyên tử R có tổng số hạt là 115, hạt mang điện nhiều hơn hạt không mang điện là 25 hạt. Cho biết cấu hình e nguyên tử của R?
A. [Ne] 3s23p3.
B. [Ne] 3s23p5.
C. [Ar] 4s24p5.
D. [Ar] 3d104s24p5
Bài giải:
Giả sử số hiệu nguyên tử, số n của R lần lượt là Z, N.
Ta có hệ phương trình như sau:
⇒ Cấu hình e của R là: [Ar] 3d104s24p5
⇒ Đáp án đúng là: C
Ví dụ 4: Chất X tạo bởi 3 nguyên tố A, B, C có công thức là ABC. Tổng số hạt cơ bản trong phân tử X là 82, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Hiệu số khối giữa B và C gấp 10 lấn số khối của A. Tổng số khối của B và C gấp 27 lần số khối của A. Tìm công thức phân tử của X?
A. HClO
B. KOH
C. NaOH
D. HBrO
Bài giải:
Gọi tổng số hạt proton và notro của phân tử X là: p, n
Ta có hệ phương trình như sau:
Gọi tổng số khối của A, B, C lần lượt là a, b, c
Ta có hệ phương trình:
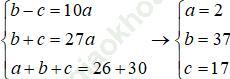
A có số khối là 2
=> pA + nA = 2,
Mà pA, nA là các số nguyên dương => pA = 1 (H)
B có số khối là 37 => pB + nB = 37
Luôn có pB ≤ nB ≤ 1,5pB; 2pB ≤ pB + nB = 37 ≤ 2,5pB
→ 14,8 ≤ pB ≤ 18,5, → pB = 15 (P), 16 (S), 17 (Cl)
C có số khối là 17 => pC + nC = 37
Luôn có pC ≤ nC ≤ 1,5 pC; 2pC ≤ pC + nC = 17 ≤ 2,5pC
→ 6≤ pC ≤ 8,5 → pC = 7 (N), 8 (O)
Để chất X có công thức ABC thì X có công thức là HClO.
⇒ Đáp án đúng là: A
Ví dụ 5: Hợp chất MX2 tạo ra từ các ion M2+ và X−. Tổng số hạt trong phân tử MX2 là 116. Số hạt trong M2+ lớn hơn số hạt trong X− là 29 hạt. Nguyên tử M có số hạt p bằng số hạt n. Nguyên tử X có số n hơn số p là 1 hạt. Xác định các nguyên tố M, X và viết công thức phân tử của hợp chất.
A. CaF2.
B. CaCl2.
C. CuF2.
D. CuCl2.
Bài giải:
Đặt số p của M và X lần lượt là p và p'
Theo bài ra ta có: p = n => Số hạt của M là: p + n + e = 3p
Do X có số n hơn số p là 1 hạt nên số hạt của X là: p' + n' + e' = 3p' + 1
Số hạt của M2+ là 3p-2 và số hạt của X− là 3p' + 1 + 1 = 3p' + 2
Số hạt M2+ lớn hơn số hạt M− là 29
⇒ 3p - 2 - (3p' + 2) = 29
⇒ p - p' = 11 (1)
Mặt khác tổng số hạt MX2 = 116
⇒ 3p + (3p' + 1) x 2 = 116 (2)
Từ (1) và (2) ⇒ p = 20; p' = 9
⇒ M là Ca; X là F ⇒ CaF2
⇒ Đáp án đúng là: A
Bài tiếp: Dạng 1: Xác định nguyên tố dựa vào số hạt - Chuyên đề Hóa 10