Bài 45 : Axit cacboxylic - Giải BT Hóa học 11
Bài 45: Axit cacboxylic
Bài 1 (trang 210 SGK Hóa 11): Thế nào là axit cacbonxylic? Viết công thức cấu tạo, gọi tên các axit có công thức phân tử C4H8O2.
Bài giải:Định nghĩa: Axit cacboxylic là những hợp chất hữu cơ mà phân tử có nhóm cacboxyl (-COOH) liên kết trực tiếp với nguyên tử cacbon(1) hoặc nguyên tử hiđro.
( (1): Nguyên tử cacbon này có thẻ của gốc hiđrocacbon hoặc của nhóm -COOH khác. )
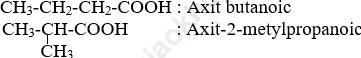
Bài 2 (trang 210 SGK Hóa 11): Từ công thức cấu tạo, hãy giải thích tại sao axit fomic có tính chất của một anđehit.
Bài giải: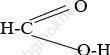
Do phân tử có nhóm –CHO nên axit fomic có tính chất của 1 anđehit
Bài 3 (trang 210 SGK Hóa 11): Từ metan và các chất vô cơ cần thiết khác có thể điều chế được axit fomic, axit axetic. Viết phương trình hóa học của các phản ứng xảy ra.
Bài giải: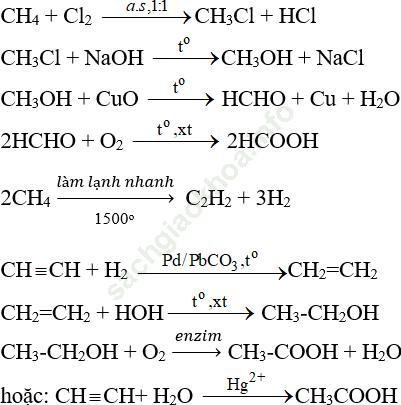
Bài 4 (trang 210 SGK Hóa 11): Chất Y có công thức phân tử C4H8O2 tác dụng với NaOH tạo thành chất Z (C4H7O2Na). Vậy Y thuộc loại hợp chất nào sau đây?
A. Anđehit;
B. Axit.
C. Ancol;
D. Xeton.
Bài giải:- Đáp án đúng là: B.
- Phương trình phản ứng:
CH3CH2CH2COOH + NaOH → CH3CH2CH2COONa + H2O
Bài 5 (trang 210 SGK Hóa 11): Để trung hòa 150,0 gam dung dịch 7,40% của axit no, mạch hở, đơn chức X cần dùng 100,0 ml dung dịch NaOH 1,50M. Viết công thức cấu tạo và gọi tên của chất X.
Bài giải:Gọi công thức phân tử của X là CnH2n+1COOH (n ≥ 1)
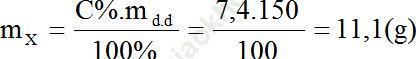
nNaOH = 0,1.1,5 = 0,15 (mol)
Phương trình phản ứng:
CnH2n+1COOH + NaOH → CnH2n+1COONa + H2O
Theo phương trình: nCnH2n+1COOH = nNaOH = 0,15 (mol)
⇒ MX = ![]() = 74
= 74
⇒ 14n + 46 = 74
⇒ n = 2 ⇒ X: C2H5COOH (axit propanoic)
Bài 6 (trang 210 SGK Hóa 11): Trung hòa 16,60gam hỗn hợp gồm axit axetic và axit fomic bằng dung dịch natri hiđroxit thu được 23,20 gam hỗn hợp hai muối.
a. Viết phương trình hóa học của các phản ứng ở dạng phân tử và ion rút gọn.
b. Xác định thành phần phần trăm khối lượng của mỗi chất trong hỗn hợp trước và sau phản ứng.
Bài giải:a) Gọi số mol của axit axetic và axit fomic lần lượt là x và y (mol)
Phương trình hoá học ở dạng phân tử:
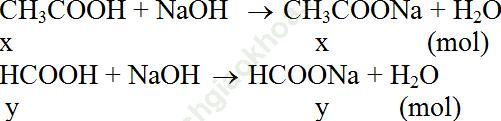
Phương trình hoá học ở dạng ion:
CH3COOH + OH- → CH3COO- + H2O
HCOOH + OH- → HCOO- + H2O
b) Theo đề bài ta có hệ phương trình:
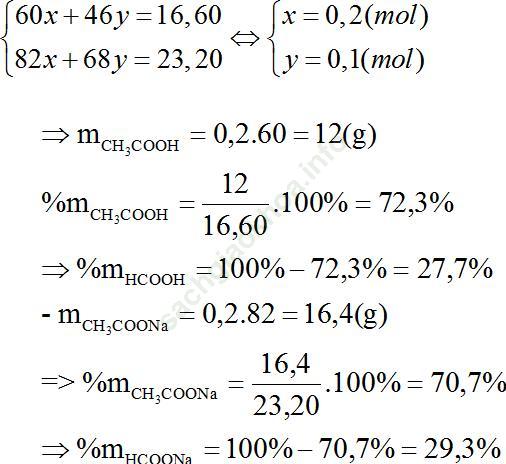
Bài 7 (trang 210 SGK Hóa 11): Đun 12,0 gam axit axetic với một lượng dư ancol etylic (có axit H2SO4 đặc làm xúc tác). Đến khi dừng thí nghiệm thu được 12,3 gam este.
a. Viết phương trình hóa học của phản ứng.
b. Tính phần trăm khối lượng của axit đã tham gia phản ứng este hóa.
Bài giải:a) Phương trình hóa học:
CH3COOH + C2H5OH ---H2SO4→ CH3COOC2H5 + H2O
b)
