Bài 15 : Cacbon - Giải BT Hóa học 11
Bài 15: Cacbon
Bài 1 (trang 70 SGK Hóa 11): Vì sao hầu hết các hợp chất của cacbon lại là hợp chất cộng hóa trị?
Bài giải:Cấu hình e của C: 1s22s22p2
C có 4e lớp ngoài, để bền vững các nguyên tố cần có 8e lớp ngoài cùng. Độ âm điện của C là 2,55 (độ âm điện trung bình) nên C khó cho hoặc nhận e một cách hoàn toàn vì vậy mà chủ yếu C hình thành liên kết với các nguyên tố khác bằng việc dùng chung các e (liên kết cộng hoá trị).
Bài 2 (trang 70 SGK Hóa 11): Tính oxi hóa của cacbon thể hiện ở phản ứng nào trong các phản ứng sau?
A. C + O2 → CO2
B. C + 2CuO → 2Cu + CO2
C. 3C + 4 Al → Al4C3
D. C + H2O → CO + H2
Bài giải:Đáp án án đúng là: C.
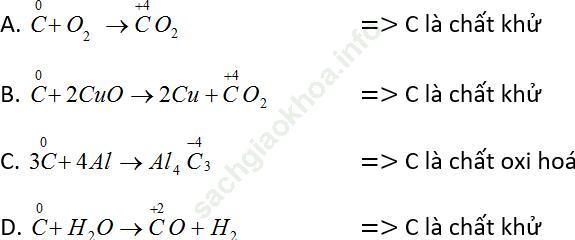
Cacbon thể hiện tính oxi hoá khi số oxi hoá giảm (tác dụng với chất khử) nên đáp án C là đúng.
Bài 3 (trang 70 SGK Hóa 11): Tính khử của cacbon thể hiện ở phản ứng nào trong các phản ứng sau?
A. 2C + Ca → CaC2
B. C + 2H2 → CH4
C. C + CO2 → 2CO
D. 3C + 4Al → Al4C3
Bài giải:Đáp án đúng là: C.
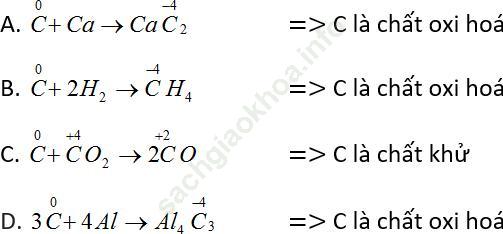
Cacbon thể hiện tính khử khi số oxi hoá tăng (tác dụng với chất oxi hoá) nên đáp án C là đúng.
Bài 4 (trang 70 SGK Hóa 11): Lập phương trình hóa học của các phản ứng sau đây:
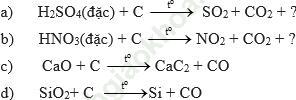
Bài giải:
Lời giải dưới thể hiện đầy đủ cả phần tăng giảm số oxi-hóa và cách cân bằng pthh:
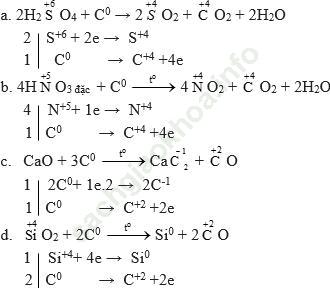
Bài 5 (trang 70 SGK Hóa 11): Đốt một mẫu than đá (chứa tạp chất không cháy) có khối lượng 0,600kg trong oxi dư, thu được 1,06 m3 (đktc) khí cacbonic. Tính thành phần phần trăm khối lượng của cacbon trong mẫu than đá trên.
Bài giải:C + O2 → CO2
47,32 ← 47,32 (mol)
Theo phương trình:
nC = nCO2 = 47,32 mol ⇒ mC = 47,32.12 = 567,84 g
% khối lượng của C là: