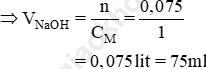Bài 11: Axit photphoric và muối photphat - Giải BT Hóa học 11
Bài 11: Axit photphoric và muối photphat
Bài 1 (trang 53 SGK Hóa 11): Viết phương trình hoá học dạng phân tử và dạng ion rút gọn của phản ứng giữa axit photphoric với lượng dư của:
a. BaO;
b. Ca (OH)2;
c. K2CO3
Bài giải:Các chất lấy dư nên muối tạo ra là muối trung hoà:
a. 2H3PO4 + 3BaO → Ba3(PO4)2 + 3H2O
Phương trình phân tử trùng với phương trình ion thu gọn
b. 2H3PO4 + 3Ca (OH)2 → Ca3(PO4)2 + 6H2O
2H3PO4 + 3Ca2+ + 6OH- → Ca3(PO4)2 + 6H2O
c. 2H3PO4 + 3K2CO3 → 2K3PO4 + 3H2O + 3CO2↑
2H3PO4 + 3CO32- → 2PO43- + 3H2O + CO2↑
Bài 2 (trang 53 SGK Hóa 11): Nêu những điểm giống và khác nhau về tính chất hoá học giữa axit nitric và axit photphoric. Dẫn ra những phản ứng hoá học để minh hoạ?
Bài giải:- Những điểm giống nhau về tính chất hóa học giữa axit nitric và axit photphoric:
- Đều có tính axit:
+ Chuyển màu chất chỉ thị: Quỳ tím chuyển thành màu hồng
+ Tác dụng với bazơ, oxit bazơ không có tính khử (các nguyên tố có số oxi hoá cao nhất):
3NaOH + H3PO4 → Na3PO4 + 3H2O
Fe2O3 + 6HNO3 → 2Fe (NO3)3 + 3H2O
+ Tác dụng với một số muối của axit yếu và không có tính khử:
2HNO3 + CaCO3 → Ca (NO3)2 + H2O + CO2↑
2H3PO4 + 3Na2SO3 → 2Na3PO4 + 3H2O + 3SO2↑
- Những tính chất khác nhau:
| HNO3 | H3PO4 |
|
- Axit HNO3 là axit mạnh HNO3 → H+ + NO3- - Axit HNO3 có tính oxi hoá mạnh Fe + 4HNO3 → Fe (NO3)3 + NO + 2H2O S + 2HNO3 → H2SO4 + 2NO 3FeO + 10HNO3 → 3Fe (NO3)3 + NO + 5H2O |
- Axit H3PO4 là một triaxit trung bình H3PO4 ⇆ H+ + H2PO4- H2PO4- ⇆ H+ + HPO42- HPO42- ⇆ H+ + PO43- - Axit H3PO4 không có tính oxi hoá. 3Fe + 2H3PO4 → Fe3(PO4)2 + 3H2 S + H3PO4 → không phản ứng 3FeO +2H3PO4 → Fe3(PO4)2 + 3H2O |
Bài 3 (trang 54 SGK Hóa 11): Phương trình điện li tổng cộng của H3PO4 trong dung dịch là:
H3PO4 ⇆ 3H+ + PO43-
Khi thêm HCl vào dung dịch:
A. Cân bằng trên chuyển dịch theo chiều thuận.
B. Cân bằng trên chuyển dịch theo chiều nghịch.
C. Cân bằng trên không bị dịch chuyển.
D. Nồng độ PO43- tăng lên.
Bài giải:- Đáp án đúng là: B.
- Khi thêm HCl vào làm tăng nồng độ H+ trong dung dịch. Theo nguyên lí chuyển dịch cân bằng, cân bằng chuyển dịch theo chiều làm giảm nồng độ H+
⇒ cân bằng chuyển dịch theo chiều nghịch.
Bài 4 (trang 54 SGK Hóa 11): Lập các phương trình hóa học sau đây:
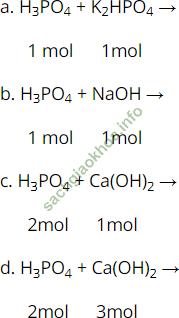
a. H3PO4 + K2HPO4 → 2KH2PO4
1 mol 1mol
b. H3PO4 + Ca (OH)2 → CaHPO4 + 2H2O
1 mol 1mol
c. 2H3PO4 + Ca (OH)2 → Ca (H2PO4)2 + 2H2O
2mol 1mol
d. 2H3PO4 + 3Ca (OH)2 → Ca3(PO4)2 + 6H2O
2mol 3mol
Bài 5 (trang 54 SGK Hóa 11): Để thu được muối photphat trung hoà, cần lấy bao nhiêu ml dung dịch NaOH 1,00M cho tác dụng với 50,0ml H3PO4 0,50M?
Bài giải:Ta có: nH3PO4 = 0,05.0,5 = 0,025 (mol)
Phương trình phản ứng:
H3PO4 + 3NaOH → Na3PO4 + 3H2O
Từ ptpư suy ra:
nNaOH = 3nH3PO4 = 3.0,025 = 0,075 (mol)