Bài 31: Tính chất - Ứng dụng của hiđro - Giải BT Hóa học 8
Bài 31: Tính chất - Ứng dụng của hiđro
Bài 1: Viết phương trình hóa học của phản ứng hiđro khử các oxit sau:
a) Sắt (III) oxit.
b) Thủy ngân (II) oxit.
c) Chì (II) oxit.
Bài giải:Các phương trình hóa học của phản ứng hiđro khử các oxit như sau:
a) Fe2O3 + 3H2 → 2Fe + 3H2O.
b) HgO + H2 → Hg + H2O.
c) PbO + H2 → Pb + H2O.
Bài 2: Nêu những ứng dụng của hiđro mà em biết.
Bài giải:Các ứng dụng của hiđro:
- Dùng làm nhiên liệu cho động cơ tên lửa, có thể làm nhiên liệu cho động cơ ô tô thay cho xăng, dùng trong đèn xì oxi - hidro để hàn cắt kim loại. Đó là vì khí hiđro cháy, sinh ra một lượng nhiệt lớn hơn nhiều lần so với cùng lượng nhiên liệu khác.
- Dùng làm chất khử để điều chế một số kim loại từ oxit của chúng.
- Là nguồn nhiên liệu trong sản xuất amoniac, axit và nhiều hợp chất hữu cơ.
- Hiđro được dùng để bơm vào khinh khí cầu, bóng thám không vì là khí nhẹ nhất.
Bài 3: Chọn cụm từ thích hợp trong khung rồi điền vào chỗ trống trong các câu sau:
Tính khử; tính oxi hóa; chiếm oxi; nhường oxi; nhẹ nhất
Trong các chất khí, hiđro là khí... Khí hidro có...
Trong phản ứng giữa H2 và CuO, H2 có... vì... của chất khác; CuO có... vì... cho chất khác.
Bài giải:Trong các chất khí, hiđro là khí nhẹ nhất. Khí hiđro có tính khử.
Trong phản ứng giữa H2 và CuO, H2 có tính khử vì chiếm oxi của chất khác, CuO có tính oxi hoá vì nhường oxi cho chất khác.
Bài 4: Khử 48 gam đồng (II) oxit bằng khí hiđro. Hãy:
a) Tìm số gam đồng kim loại thu được.
b) Xác định thể tích khí hiđro (đktc) cần dùng.
Bài giải:a) Ta có:
nCuO = ![]() = 0,6 mol.
= 0,6 mol.
Phương trình hóa học của phản ứng khử CuO như sau:
CuO + H2 → Cu + H2O.
Ta có: nCu = 0,6mol.
mCu = 0,6.64 = 38,4g.
Vậy số gam đồng kim loại thu được là 38,4g.
b)
Theo phương trình phản ứng trên ta có:
nH2 = 0,6 mol
VH2 = 0,6.22,4 = 13,44 lít.
Vậy thể tích khí hiđro (đktc) cần dùng là: 13,44 lít.
Bài 5: Khử 21,7 gam thủy ngân (II) oxit bằng hiđro. Hãy:
a) Tìm số gam thủy ngân thu được.
b) Xác định số mol và thể tích khí hiđro (đktc) cần dùng.
Bài giải:a) Ta có:
nHgO = ![]() = 0,1 mol.
= 0,1 mol.
Phương trình hóa học của phản ứng khử HgO như sau:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1.201 = 20,1g.
Vậy số gam thủy ngân thu được là: 20.1g
b) Ta có: nH2 = 0,1 mol.
VH2 = 0,1.22,4 = 2,24l.
Vậy số mol hiđro (đktc) cần dùng là: 0.1 mol
Thể tích khí hiđro (đktc) cần dùng là: 2.24l
Bài 6: Xác định số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít oxi (các thể tích đo ở đktc).
Bài giải: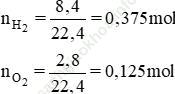
Phương trình hóa học của phản ứng tạo nước như sau:
2H2 + O2 → 2H2O.
So sánh tỉ lệ: ![]()
Theo phương trình trên ta có:
nH2O = 2.0,125 = 0,25 mol.
mH2O = 0,25.18 = 4,5g.
Vậy số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít oxi là 4.5g